アクチン細胞骨格の制御機構に関する研究
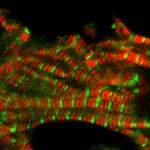
細胞骨格は、その構成因子である単量体の重合・脱重合によりダイナミックにその構造を変化させて、細胞運動をひきおこす。中でもアクチン細胞骨格は、重合した直線状のアクチン線維がミオシン線維と「収縮装置」を形作ることで効率的な力の発生が可能となり、細胞レベルでの形態変化のみならず個体レベルでの運動・姿勢制御から呼吸・循環といった生命機能の本質部分を担っている。このアクチン収縮装置の収縮メカニズムはこれまでの研究により基本的に解明されてきたが、収縮装置の形成・維持機構に関する知見は非常に乏しい。収縮装置を構成する直線状のアクチン線維も、重合により形成・維持されており、そのアクチン重合は厳密に制御されていると考えられるが、その詳細はほぼ未解決である。 私達は、収縮装置形成におけるアクチン重合の分子機構を中心に、アクチン収縮装置の形成と恒常性維持のメカニズム解明に挑んでいる。
代表論文
Matsuyama S, Kage Y, Fujimoto N, Ushijima T, Tsuruda T, Kitamura K, Shiose A, Asada Y, Sumimoto H, Takeya R. Interaction between cardiac myosin-binding protein C and formin Fhod3. Proc Natl Acad Sci U S A. 2018 ; 115: E4386-95. doi: 10.1073/pnas.1716498115.
Ushijima T, Fujimoto N, Matsuyama S, Kan-o M, Kiyonari H, Shioi G, Kage Y, Yamasaki S, Takeya R, Sumimoto H. The actin-organizing formin protein Fhod3 is required for postnatal development and functional maintenance of the adult heart in mice. J Biol Chem. 2018;293:148-162.
Kan-O M, Takeya R, Abe T, Kitajima N, Nishida M, Tominaga R, Kurose H, Sumimoto H. Mammalian formin Fhod3 plays an essential role in cardiogenesis by organizing myofibrillogenesis. Biol Open. 2012;1:889-96.
Kan-o M, Takeya R, Taniguchi K, Tanoue Y, Tominaga R, Sumimoto H. Expression and subcellular localization of mammalian formin Fhod3 in the embryonic and adult heart. PLoS One. 2012;7(4):e34765.
Taniguchi K, Takeya R, Suetsugu S, Kan-O M, Narusawa M, Shiose A, Tominaga R, Sumimoto H. Mammalian formin fhod3 regulates actin assembly and sarcomere organization in striated muscles. J Biol Chem. 2009 ; 284:29873-81.
インスリン受容体シグナリングに関する研究
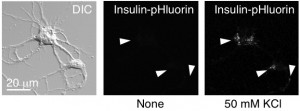
脳内のインスリンはインスリン受容体シグナルを活性化することで、神経回路網の形成・維持・修復を促し、代謝障害や炎症反応に起因するさまざまなストレスから神経を保護している。アルツハイマー型認知症発症時、記憶・学習を司る海馬領域において、インスリンの遺伝子発現やインスリン受容体シグナルの機能は破綻している。アミロイドβ凝集による老人班やタウ過剰リン酸化に伴う神経原線維変化などを起因とするアルツハイマー病で、インスリン分泌不全やインスリン抵抗性様の病態生理学的変化が脳内で確認された。それらの病理学的変化を認めた脳は、代謝障害や炎症反応に起因されるさまざまなストレスに対してきわめて脆弱であり、アルツハイマー病の進行をさらに加速させると言われている。私たちは未だ解明されていない「アルツハイマー病態時のインスリン分泌不全やインスリンシグナル機能不全の詳細なメカニズム」について解析をおこなっている。
代表論文
Nemoto T, Toyoshima-Aoyama F, Yanagita T, Murata T, Fujita H, Koshida T, Yonaha T, Wada A, Sawaguchi A, Murakami M. New insights concerning insulin synthesis and its secretion in rat hippocampus and cerebral cortex: Amyloid-β1-42-induced reduction of proinsulin level via glycogen synthase kinase-3β. Cellular Signal. 2014; 26: 253-259.