血管内灌流固定法
Fixation by vascular perfusion
灌流固定はマウスやラットなどの小動物に麻酔をかけた状態で、心臓の左心室から固定液を注入するもので、手技に一定の熟練を要しますが、細胞や組織が生きた状態で固定液が末梢血管に行き渡ることから、良好な固定条件を得ることができます。
ラット1匹当たりの溶液量
生理食塩水 100 ml/固定液 100 ml(血管内灌流用)/固定液 60 ml (追加浸漬固定用)
はじめに点滴台にかけた2つの容器に生理食塩水(容器A)と固定液(容器B)を入れ、チューブ内の空気を除いた後、三方活栓を操作して容器Aから生理食塩水が流れ出る状態にしてストッパーをかけておきます。
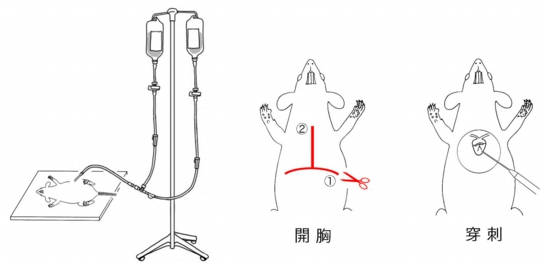
麻酔が十分に効いていることを確認した後、上図の切開線に沿って開胸します。
続いて、拍動する心臓の心尖部から左心室に注射針(18G)を穿刺し(注射針の先端が左心室を突き抜けず、心室内に位置するように注意)、注射針が抜けないよう鉗子などで心筋の上から挟み留めます。次に血液と灌流液を排出するため、右心房の一部を切開し、直ちにストッパーを開放して生理食塩水を注入します。
血液の排出が進むにつれ、肝臓が赤色からピンク色に変化し、右心房から排出される液が透明化していきます。約30秒が経過して、十分に血液が排出されたことを確認した後、三方活栓を切り換えて固定液を注入します。
固定液が環流すると筋肉が収縮し、次第に固定が進行していきます。ラット1匹あたり80〜100 mlの固定液を環流し、注射針を抜去した後、観察を行う臓器・組織を切除し、2 mm〜3 mm 四方程度に細切して追加浸漬固定液に浸します。

電子顕微鏡用試料サイズ
室温で約2時間または冷蔵で一晩、追加浸漬固定後、固定液を0.1M リン酸緩衝液に置き換えて冷蔵保存し、必要に応じて次の試料作製行程へ進みます(数ヶ月間、保存可能)。
マウス1匹当たりの溶液量
生理食塩水 40 ml/固定液 40 ml(血管内灌流用)/固定液 30 ml (追加浸漬固定用)
マウスの場合は21Gまたは23Gの注射針を使用し、点滴台の代わりに生理食塩水と固定液を別々に充填した50 mlシリンダを差し替えて注入する変法をとることが出来ます。